Acide nitrilotriacétique
L'acide nitrilotriacétique est un acide tricarboxylique de formule brute C 6 H 9 N 1 O 6. Le NTA peut se lier avec les ions métalliques, par réaction chimique de complexation, et forme ainsi des complexes hydrosolubles.

Catégories :
Acide carboxylique - Cancérogène du groupe 2B du CIRC - Agent chélatant - Chélation - Chimie analytique
Recherche sur Google Images :
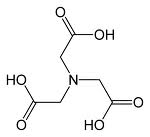
Source image : fr.academic.ru Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Page(s) en rapport avec ce sujet :
- Le Centre International de Recherche sur le Cancer (CIRC) considère que l'acide nitrilotriacétique et ses sels peuvent être cancérogènes pour l'homme... (source : reptox.csst.qc)
- AB-076 Détermination polarographique de l'acide nitrilotriacétique (NTA) et de l'acide éthylènediaminetétraacétique (EDTA) selon la norme DIN 38413 partie 5... (source : interchimie)
- Acide nitrilotriacétique - Alfa Æsar GmbH & Co. KG. (source : fr.exportpages)
| Acide nitrilotriacétique | |
|---|---|
 |
|
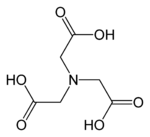
| Structure 2D de l'acide nitrilotriacétique | |
| Général | |
| Nom IUPAC | acide 2-[bis (carboxyméthyl) amino]acétique |
| No CAS | |
| No EINECS | |
| PubChem | |
| SMILES |
|
| InChI |
|
| Apparence | poudre cristalline blanche[1] |
| Propriétés chimiques | |
| Formule brute | C6H9NO6 [Isomères] |
| Masse molaire[3] | 191, 1388 ± 0, 0074 g·mol-1 C 37, 7 %, H 4, 75 %, N 7, 33 %, O 50, 22 %, |
| pKa | 3, 03 à 23 °C [2] |
| Propriétés physiques | |
| T° fusion | 242 °C (Décomposition) [4] |
| Solubilité | 1, 28 g·l-1 (eau, 22, 5 °C) [4] |
| Point d'éclair | 100 °C [4] |
| Thermochimie | |
| ΔfH0solide | -1 311, 9 kJ·mol-1 [5] |
| Précautions | |
|
|
|
| Produit non classifié | |
|
|
|
| Groupe 2B : Peut-être cancérogène pour l'homme[6] | |
| Écotoxicologie | |
| DL50 | 3 160 mg·kg-1 (souris, oral) 1 100 mg·kg-1 (rat, oral) [2] |
| LogP | -3, 8[1] |
|
|
|
L'acide nitrilotriacétique (noté aussi NTA) est un acide tricarboxylique de formule brute C6H9N1O6. Le NTA peut se lier avec les ions métalliques, par réaction chimique de complexation, et forme ainsi des complexes hydrosolubles. C'est un agent chélateur important qui trouve de nombreuses applications industrielles. Les impacts du NTA vis-à-vis de la santé des mammifères et de la toxicité environnementale sont décrits par une revue scientifique de 1985 [8].
Notes et références
- ACIDE NITRILOTRIACETIQUE, fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- (en) «Nitrilotriacetic acid» sur ChemIDplus, consulté le 16 février 2009
- Masse molaire calculée selon Atomic weights of the elements 2007 sur www. chem. qmul. ac. uk
- Entrée de «Nitrilotriacetic acid» dans la base de données de produits chimiques GESTIS de la BGIA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 16 février 2009 (JavaScript indispensable)
- Nitrilotriacetic acid sur http ://www. nist. gov/. Consulté le 16 février 2009
- IARC Working Group on the Evaluation of Carcinogenic Risks to Humans, «Evaluations Globales de la Cancérogénicité pour l'Homme, Groupe 2B : Peut-être cancérogènes pour l'homme» sur http ://monographs. iarc. fr, CIRC, 16 janvier 2009. Consulté le 22 août 2009
- «Acide nitrilotriacétique» dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Anderson, R. L., Bishop, W. E. et Campbell, R. L. A review of the environmental and mammalian toxicology of nitrilotriacetic acid. CRC Crit. Rev. Toxicol., 15 (1) : 1 (1985)
Recherche sur Amazone (livres) : |
Principaux mots-clés de cette page :
acide - 2009 - chimiques - nitrilotriacétique - sécurité - nitrilotriacetic - acid - consulté - produit - homme - nta - santé - propriétés - formule - brute - masse - molaire - mol - 100 - circ -
Ce texte est issu de l'encyclopédie Wikipedia. Vous pouvez consulter sa version originale dans cette encyclopédie à l'adresse http://fr.wikipedia.org/wiki/Acide_nitrilotriac%C3%A9tique.
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 30/11/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 30/11/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.

 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité